„Żywy lek” dla dzieci z białaczką

Opublikowano 5 września 2018 12:40
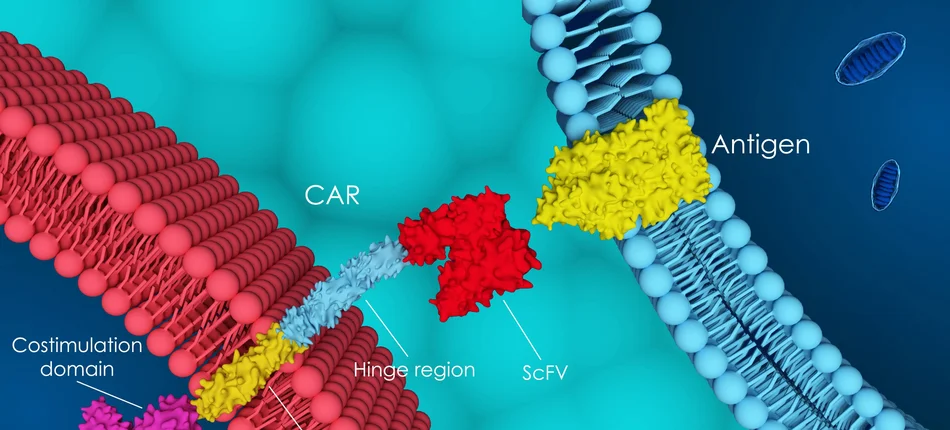
Komisja Europejska (KE) zarejestrowała tisagenlekleucel – terapię komórkową CAR-T firmy Novartis. Rejestracja obejmuje dwa wskazania:
- leczenie pacjentów pediatrycznych i młodych dorosłych w wieku do 25 lat z oporną ostrą białaczką limfoblastyczną z komórek B (ALL) w nawrocie choroby po transplantacji szpiku lub w drugim bądź kolejnym rzucie leczenia;
- leczenie dorosłych pacjentów z chłoniakiem rozlanym z dużych limfocytów B (DLBCL) w postaci nawrotowej lub opornej (r/r) po co najmniej dwóch liniach terapeutycznych.
Zarówno ALL z komórek B, jak i DLBCL są agresywnymi, złośliwymi nowotworami krwi.
Tisagenlekleucel to terapia typu CAR-T, produkowana indywidualnie dla każdego pacjenta poprzez przeprogramowanie jego własnych limfocytów T do walki z nowotworem. To obecnie jedyna terapia chimerycznym receptorem antygenu limfocytu T (CAR-T), która uzyskała zatwierdzenie Komisji Europejskiej w dwóch typach nowotworów komórek B. To także pierwsza terapia komórkowa CAR-T zatwierdzona przez Amerykańską Agencję ds. Żywności i Leków (FDA).
Decyzja KE została oparta na wynikach dwóch globalnych badań klinicznych – JULIET i ELIANA, w których udział wzięli pacjenci z ośmiu krajów europejskich. W badaniach tych tisagenlekleucel wykazał silne i trwałe wskaźniki odpowiedzi na leczenie oraz stały profil bezpieczeństwa w dwóch trudnych do leczenia typach agresywnego nowotworu krwi.
– Kiedy Uniwersytet Pensylwanii i Novartis zdecydowały się współpracować w celu opracowania terapii CAR-T, nasz główny cel był jasny i ambitny – zaspokoić potrzeby pacjentów, ratować ich życie i poprawić jego jakość – mówi dr n.med. Carl June z Katedry Patologii i Medycyny Laboratoryjnej w Penn oraz Centrum Immunoterapii Komórkowej w Centrum Onkologicznym Abramsona. – Jesteśmy dumni, że nasze wysiłki w rozwoju terapii CAR-T przynoszą pacjentom cierpiącym na nowotwory krwi przełom, który daje nową nadzieję.
– Udostępnienie tisagenlekleucel pacjentom w UE to niespotykany dotąd postęp w leczeniu, który młodym pacjentom z ALL, leczonym dotychczas bezskutecznie dostępnymi terapiami i mającym ograniczone dalsze możliwości leczenia, oferuje terapię, która może uratować ich życie - stwierdził prof. Peter Bader z Zakładu Transplantacji Komórek Macierzystych i Immunologii oraz główny badacz ELIANA w Szpitalu Uniwersyteckim dla Dzieci i Młodzieży we Frankfurcie nad Menem.
Terapia ta może jednak powodować działania niepożądane, które mogą być ciężkie lub zagrażać życiu. Dlatego dostępność leku tisagenlekleucel w każdym kraju będzie zależeć od wielu czynników, w tym od dostosowania wykwalifikowanych ośrodków leczenia, a także od postępowania refundacyjnego.
Ostra białaczka limfoblastyczna (ALL) stanowi w Europie około 80% wszystkich przypadków zachorowań na białaczkę wśród dzieci. Rokowania pacjentów z nawrotem choroby po standardowej terapii są bardzo złe. Pomimo stosowania u pacjentów licznych terapii, takich jak chemioterapia, radioterapia, terapia celowana czy przeszczep komórek macierzystych wskaźnik przeżycia jest niski, co potęguje potrzebę nowych opcji leczenia.
Z kolei chłoniak rozlany z dużych komórek B to najczęstsza postać chłoniaka nieziarniczego, globalnie stanowiąca nawet do 40% przypadków zachorowań. U pacjentów, u których nastąpił nawrót choroby lub wystąpił brak odpowiedzi na pierwotną terapię, opcje leczenia dające trwałe odpowiedzi są ograniczone. Dla większości pacjentów wskaźniki przeżycia są niskie ze względu na to, iż nie kwalifikują się oni do autologicznego przeszczepu komórek macierzystych (ASCT) lub przeszczep ten czy chemioterapia ratunkowa nie powiodły się.
Źródło: inf. pras.
Tematy
białaczka / DLBCL / chłoniaki / ALL / CAR-T / Peter Bader / Carl June / tisagenlekleucel / terapie komórkowe / żywe leki